VAMOS A POR LA RESISTENCIA BACTERIANA
PROYECTO 2023

VAMOS A POR LAS INFECCIONES BACTERIANAS
Queremos desarrollar estrategias novedosas para poder tratar las infecciones y enfermedades provocadas por bacterias resistentes a los tratamientos con antibióticos.
Ahora, con el programa Faster Future, tú puedes ayudarnos a acelerar esta investigación.
También puedes hacer tu donativo con Bizum
CÓDIGO: 33355
TU DONACIÓN DESGRAVA
LAS DONACIONES TIENEN IMPORTANTES VENTAJAS FISCALES
MÁS DE 150 €
A partir de 150 €/año podrás desgravarte el 65% de tu donación.
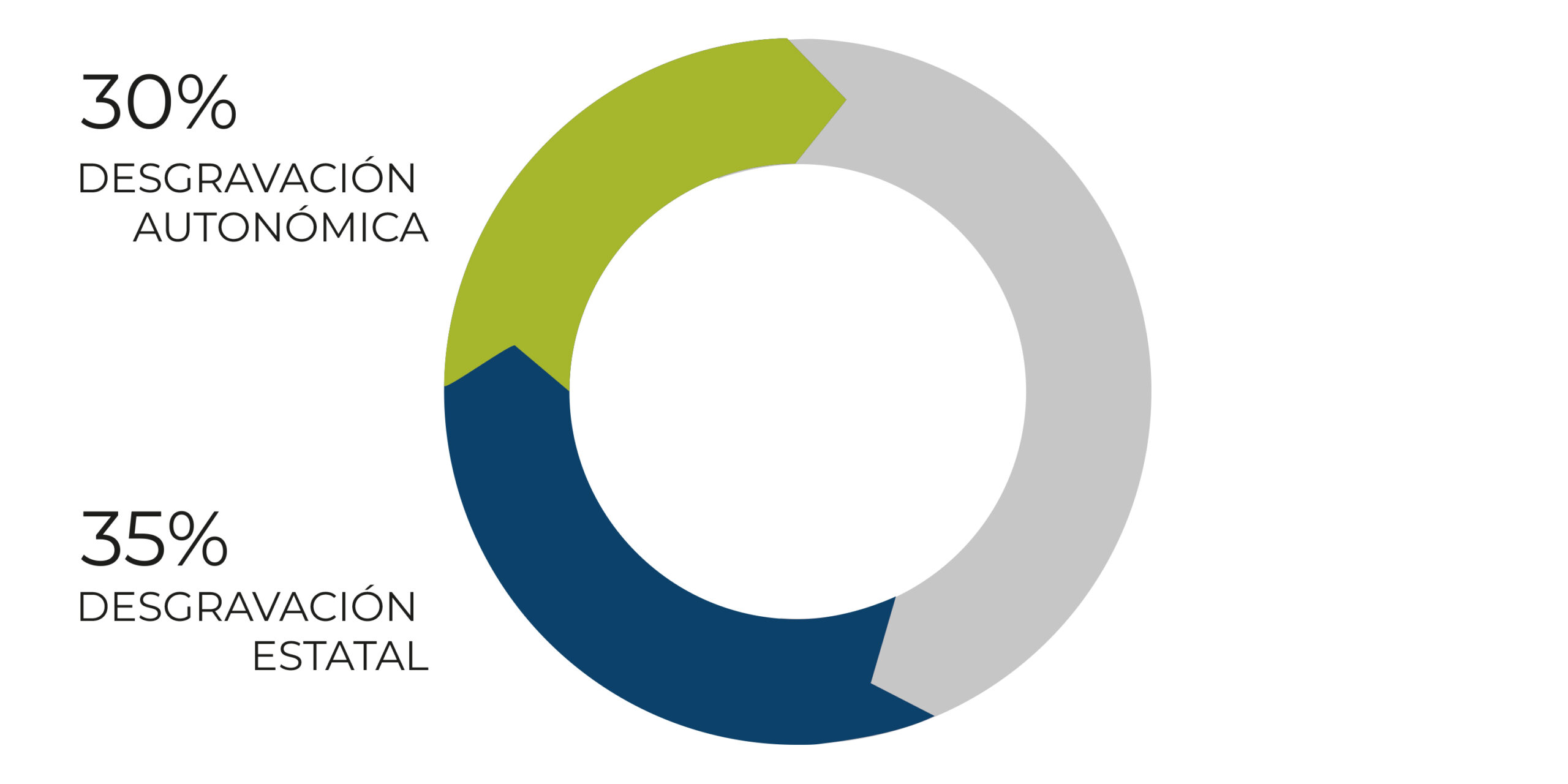
35% desgravación estatal + 30% desgravación autonómica (en Cataluña)


HAZTE SUPERAMIGO/A DEL IBEC
TUS DATOS:
SER SUPERAMIGO/A DEL IBEC TIENE MUCHAS VENTAJAS!
- Serás el primero en recibir el último número de nuestro cómic sobre IBBI, la superheroína científica.
- Podrás venir a las visitas que organizamos a nuestros laboratorios.
- Tendrás inscripción preferente a los talleres de ciencia.
- Estarás informado/a sobre los últimos descubrimientos y avances en bioingeniería.
- Tendrás toda la información sobre ferias, conferencias y eventos de divulgación en bioingeniería.
OTRAS FORMAS DE COLABORAR
CAMPAÑAS SOLIDARIAS
Ponte en contacto con nosotros, te ayudaremos a organizar tu campaña solidaria.
Solo tienes que enviarnos un email y hacer tu propuesta a:
donaciones@ibecbarcelona.org
LEGADO SOLIDARIO
Dejando tu legado al Instituto de Bioingeniería de Cataluña contribuirás a acelerar la investigación en salud.
Ponte en contacto con nosotros:
donaciones@ibecbarcelona.org



